
일부 국가에서 코로나19 치료제로 사용하고 있는 ‘렘데시비르’의 국내 수입이 승인됐다.
식품의약품안전처는 다국적 제약사 길리어드가 코로나19 치료제로 개발 중인 렘데시비르에 대해 특례수입을 결정했다고 3일 밝혔다.
의약품 특례수입 제도는 감염병 대유행 등 공중보건 위기상황에 대처하기 위해 관계 부처장의 요청에 따라 식약처장이 국내 허가되지 않은 의약품을 수입자를 통해 수입토록 하는 제도다.
식약처는 “렘데시비르 사용에 따른 중증환자의 치료기간 단축은 임상적으로 의미가 있고, 선택 가능한 치료제의 추가적인 확보가 필요한 것으로 판단했다”며 “현재 미국‧일본‧영국에서도 렘데시비르를 코로나19 팬데믹 상황에서 사용토록 한 점도 고려했다”고 승인 이유를 설명했다.
이에 따라 질병관리본부는 식약처 등 관계부처, 렘데시비르 수입자인 길리어드사이언스코리아와 국내 수입을 협의할 예정이다.
질병관리본부는 신종감염병 중앙임상위원회가 코로나19 치료제로서 렘데시비르의 국내 도입을 제안함에 따라 식약처에 특례수입을 요청한 바 있다.
이에 식약처는 국가필수의약품 안정공급 협의회(질병관리 분과위원회)의 심의를 거쳐서 특례수입을 결정했다.
정부는 국내 렘데시비르 수입자인 길리어드사이언스코리아와 함께 해당 의약품이 빠른 시일 내에 수입할 수 있도록 지원한다는 방침이다.
▶‘렘데시비르’ 주요 특징
[제품 개요]
① 주성분
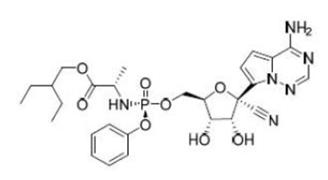
렘데시비르는 뉴클레오시드 리보핵산(ribonucleic acid; RNA) 중합효소 억제제이다. 렘데시비르의 화학명은 2-ethylbutyl N-(S)-[2-C-(4-aminopyrrolo [2,1-f][1,2,4] triazin-7-yl)-2,5-anhydro-d-altrononitril-6-Oyl]phenoxyphosphoryl–L-alaninate이다. 렘데시비르의 구조식은 다음과 같으며, 분자식은 C27H35N6O8P, 분자량은 602.6 g/mol이다.
② 제형 및 함량
* 주사용 동결건조분말 100mg : 각 단회 용량 바이알에는 멸균 상태의 백색 내지 미백색 내지 황색의 동결건조 분말이 들어 있으며, 보존제는 함유하지 않는다. 멸균 주사용수 19mL로 재구성하고, 0.9% 멸균생리식염수로 희석해서 투여한다. 재구성 후에는 5mg/mL 용액 20mL로 렘데시비르 100mg을 함유한다.
*주사용 용액 5 mg/mL : 무색 내지 황색의 투명한 용액으로서 5mg/mL 용액 20mL로, 렘데시비르 100mg을 함유하며, 보존제는 함유하지 않는다.
③ 성상
* 주사용 동결건조분말 100mg : 백색‧미백색 또는 황색 가루로, 단회 용량의 투명한 유리 바이알로 공급된다.
* 주사용 용액 5 mg/mL : 무색 내지 황색의 투명한 수용액으로, 단회 용량 투명 유리 바이알로 공급된다.
④ 첨가제
베타덱스설포부틸에테르나트륨(sulphobutyl Ether β-cyclodextrin sodium; SBECD), 주사용수, 염산 또는 수산화나트륨(pH 조절제)를 함유한다. 주사용 동결건조분말 100mg은 3g의 SBECD를, 주사용 용액 5 mg/mL은 6g의 SBECD를 포함한다.
[효능‧효과]
PCR 검사 등을 통해 코로나바이러스감염증-19가 확진된 환자로서 △실내공기(room air)에서 산소포화도(SpO2) 94% 이하인 환자 △보조산소 치료가 필요한 환자 △비침습적 또는 침습적 기계환기나 체외막산소요법(ECMO)이 필요한 환자 등 3가지 중 1가지 이상 해당하는 중증 입원 환자에게 효능을 보인다.
[용법‧용량]
투여하기 전 간기능 및 신장기능 검사를 실시해서 투여 여부를 판단한다. 이 약 투여 기간 중에도 매일 간기능을 모니터링해서 이 약의 투여 지속 여부를 평가한다. eGFR이 30mL/min/1.73m2 미만(7일 이상, 28일 이하인 신생아의 경우 혈청 크레아티닌 1mg/dL 이상)이거나 ALT가 정상상한치의 5배 이상인 경우에는 투여가 권장되지 않는다.
[투여 용량]
* 성인 : 이 약의 권장용량은 첫째 날 200mg 투여 후 둘째 날부터 100mg 투여한다.
* 소아 : 소아에서 코로나19에 대한 이 약의 치료 효과는 평가된 바 없으며, 소아에서의 약동학 정보는 없다. 소아에서의 권장 용량은 건강한 성인에서의 약동학 정보를 바탕으로 생리학 기반 약물동태(PBPK‧Physiologically Based pharmacokinetic) 모델링을 통해 산출됐다. 이 약을 투여해서 기대되는 임상적 유익성이 위해성을 상회하는 경우에만 이 약을 투여한다.
* 체중 40 kg 이상 소아 : 이 약의 권장용량은 첫째 날 200mg 투여 후 둘째 날부터 100mg이다.
* 체중 3.5 kg 이상 40 kg 미만 소아 : 이 약의 권장용량은 첫째 날 5mg/kg 투여 후 둘째 날부터 2.5mg/kg이다.
[투여 기간]
침습적 기계환기나 체외막산소요법(ECMO)이 필요한 환자에서의 권장 투여기간은 10일이다. 침습적 기계환기나 체외막산소요법(ECMO)이 필요하지 않은 환자에서는 권장 투여기간을 5일로 하고, 5일 투여 후 임상 증상이 개선되지 않는 경우 추가로 5일간 투여(100mg)할 수 있다. 전체 투여기간은 10일 이내로 한다.
[투여 방법]
30분에서 120분에 걸쳐 1일 1회 점적 정맥 투여(IV infusion)하며, 근육주사(IM)를 하지 않는다. 보존제를 함유하지 않으며, 단회 용량 바이알의 미사용 부분은 희석 용액을 조제한 후 폐기해야 한다. 주사용 액제는 체중 3.5 kg 이상, 40 kg 미만 소아에게는 사용하지 않으며 주사용 동결건조분말만을 사용한다.


